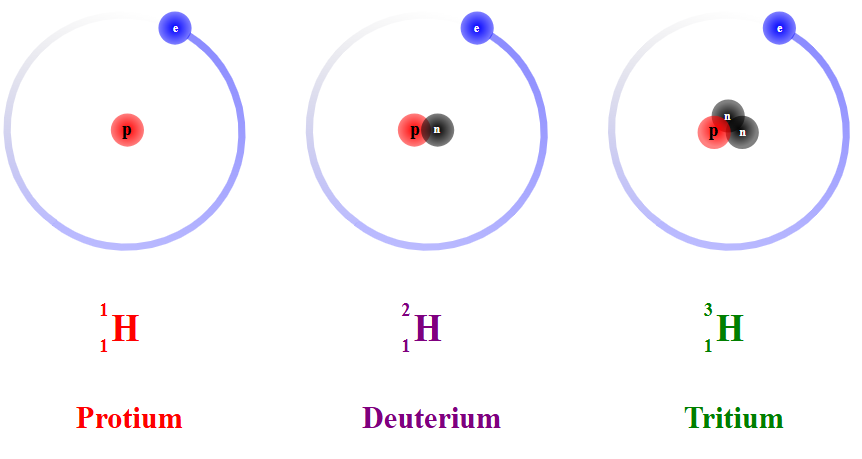
আইসোটোপের ক্ষেত্রে কোনটি সঠিক?
-
ক
ভরসংখ্যা
-
খ
নিউট্রন সংখ্যা একই থাকে
-
গ
প্রোটন সংখ্যা সমান থাকে
-
ঘ
প্রোটন ও নিউট্রন সংখ্যা সমান থাকে
আইসোটোপ হল একই মৌলিক পদার্থের ভিন্ন ভিন্ন পরমাণু যাদের পারমাণবিক সংখ্যা একই তবে নিউক্লিয়াসে নিউট্রনের সংখ্যা ভিন্ন। সমস্থানিকসমূহের পারমাণবিক সংখ্যা একই কিন্তু ভর সংখ্যা ভিন্ন। প্রোটনের সংখ্যা একই থাকায় সমস্থানিকসমূহের রাসায়নিক ও ভৌত ধর্মে অনেক সাদৃশ্য বিদ্যমান। যেমন - কার্বন - ১২, কার্বন - ১৩, কার্বন - ১৪ তিনটি সমস্থানিক যারা একই পদার্থ কার্বন হতে উৎপন্ন, এদের ভর সংখ্যা যথাক্রমে ১২, ১৩ ও ১৪। কার্বনের পারমাণবিক সংখ্যা ৬, তাই এসকল সমস্থানিকে নিউট্রনের সংখ্যা হল যথাক্রমে ১২ - ৬ = ৬, ১৩ - ৬ = ৭ এবং ১৪ - ৬ = ৮। সংক্ষেপে, সমস্থানিকসমূহ ভিন্ন নিউট্রন সংখ্যা বিশিষ্ট একই পদার্থের পরমাণু। এদের প্রোটন ও ইলেকট্রন সংখ্যা একই।
Related Question
View All-
ক
50%
-
খ
99.3%
-
গ
0%
-
ঘ
69.3%
-
ক
-
খ
-
গ
-
ঘ
-
ক
৮
-
খ
১৭
-
গ
৯
-
ঘ
২৫
-
ক
এটম শব্দের অর্থ হলো পরমাণু। পরমাণু রাসায়নিক বিক্রিয়া অংশ গ্রহণ করে। এদের স্বাধীন অস্তিত্ব নেই। যে সকল পরমাণূ বা মৌলের প্রোটন সংখ্যা একই কিন্তু ভর সংখ্যা ভিন্ন তাদের আইসোটপ বলে। এরা একই মৌলের পরামণু
-
খ
-
-
গ
-
-
ক
ইলেকট্রন
-
খ
প্রোটন
-
গ
নিউট্রন
-
ঘ
কারণ অনাবিষ্কৃত
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!
Related Question
Question Analytics
মোট উত্তরদাতা
জন